¿Por qué no se fabrica agua masivamente si conocemos su fórmula molecular?
La crisis del agua nos exige trabajar en nuevas tecnologías para la reutilización del recurso más preciado para la vida. Pero, tal vez te pusiste a pensar por qué directamente no la creamos desde cero en laboratorios, si ya sabemos que H2O es su "receta".

Sabemos de la existencia de varios métodos físicos y químicos de captación, desalinización, purificación, potabilización y redistribución del agua, para poder reutilizar este recurso vital. A pesar de que las tecnologías lograr avanzar en esta área con métodos mejorados cada vez más eficientes, no es suficiente y la crisis del agua sigue escalando.
De la unión de dos átomos de hidrógeno (H) y uno de oxígeno (O) se obtiene: H2O (monóxido de dihidrógeno), que es la fórmula molecular del agua. Tenemos los ingredientes disponibles pero, evidentemente, alguno de los pasos de “esta receta” no debe ser simple de realizar en un laboratorio, y existen motivos para no crearla masivamente.
¿Es posible fabricar agua?
Sí, el proceso de “fabricación” del agua desde cero es posible, pero hay una (o dos) razones fundamentales por las cuales no se hace de forma masiva. Por eso, la ciencia está continuamente buscando alternativas tecnológicas para lograr el mejor método de reutilización del agua, porque no somos capaces de crear fuentes inagotables de “agua nueva artificial” a gran escala, y mucho menos de instalarlas en puntos del planeta estratégicos para terminar con la crisis hídrica. Te contamos por qué no se fabrica agua desde cero.
Creación del agua: electrólisis y fotolisis
El agua en el laboratorio puede lograrse mediante dos procesos principales: la electrólisis y la fotólisis.
La electrólisis es el proceso mediante el cual se divide el agua en sus componentes básicos, oxígeno e hidrógeno, mediante la aplicación de una corriente eléctrica. El oxígeno se libera en un electrodo y el hidrógeno en el otro. Estos dos gases pueden entonces ser recolectados y recombinados para crear agua nuevamente. Este proceso es utilizado en algunas aplicaciones industriales, como la producción de hidrógeno como combustible.

Por otro lado, la fotolisis implica la separación del agua en sus componentes básicos mediante la exposición a la luz. Esto se logra mediante el uso de un fotocatalizador, que es un material que absorbe la luz y cataliza la reacción química. El oxígeno y el hidrógeno pueden entonces ser recolectados de la misma manera que en la electrólisis.
No es viable pensar en la producción de agua a gran escala mediante estos métodos, ya que la reacción que hay que desatar tiene por un lado un gran costo económico, y además, libera una enorme cantidad de energía extremadamente peligrosa que podría crear explosiones colosales.
En ambos métodos de creación se requiere una enorme cantidad de energía con lo cual, este proceso deja de ser eficiente y es extremadamente peligroso. Sin embargo, estos procesos son esenciales en algunas aplicaciones industriales y pueden tener implicaciones importantes en la investigación sobre tecnologías verdes y en la producción de combustibles limpios.
Avances en la producción del agua
Los científicos han trabajado durante años para encontrar distintas formas de crear agua, un grupo destacado del Departamento de Química, de la Universidad de Illinois, EE.UU. publicado en el año 2007, descubrió una nueva manera de producir agua evitando una gran explosión. De todas maneras, este proceso sigue resultando muy costoso y tampoco es eficiente, pero puede usarse para otra finalidad destacada.
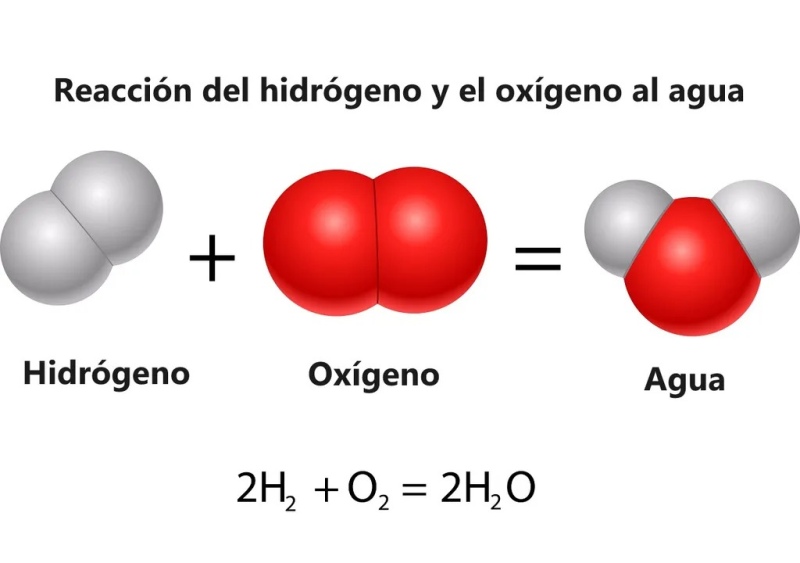
“La reacción (2H2 + O2 = 2H2O + Energía) se conoce desde hace siglos, pero hasta ahora nadie la había hecho funcionar en una solución homogénea”, dijo Thomas Rauchfuss, profesor de química de dicha Universidad y autor principal del artículo.
La conocida reacción también describe lo que sucede dentro de una pila de combustible de hidrógeno. En una celda de combustible típica, el gas hidrógeno diatómico (H2) ingresa por un lado de la celda y el gas oxígeno diatómico (O2) ingresa por el otro lado.

Las moléculas de hidrógeno pierden sus electrones y quedan cargadas positivamente mediante un proceso llamado oxidación, mientras que las moléculas de oxígeno ganan cuatro electrones y quedan cargadas negativamente mediante un proceso llamado reducción. Los iones de oxígeno cargados negativamente se combinan con iones de hidrógeno cargados positivamente para formar agua y liberar energía eléctrica.
El "lado difícil" de la pila de combustible es la reacción de reducción de oxígeno, no la reacción de oxidación de hidrógeno, dijo Rauchfuss. "Sin embargo, descubrimos que nuevos catalizadores para la reducción de oxígeno también podrían conducir a nuevos medios químicos para la oxidación del hidrógeno".
Rauchfuss y Heiden investigan recientemente una generación relativamente nueva de catalizadores de hidrogenación por transferencia para su uso como hidruros metálicos no convencionales para la reducción de oxígeno.
Estos investigadores se centran en la reactividad oxidativa de los catalizadores de hidrogenación por transferencia a base de iridio en una solución homogénea no acuosa. Descubrieron que el complejo de iridio afecta tanto a la oxidación de los alcoholes como a la reducción del oxígeno .
"La mayoría de los compuestos reaccionan con hidrógeno u oxígeno, pero este catalizador reacciona con ambos", dijo Heiden. “Reacciona con hidrógeno para formar un hidruro y luego reacciona con oxígeno para formar agua; y lo hace en un cartucho homogéneo y no acuoso”. Los nuevos catalizadores podrían conducir al desarrollo final de pilas de combustible de hidrógeno más eficientes, reduciendo sustancialmente su costo, dijo Heiden.
La solución es: no contaminar el agua
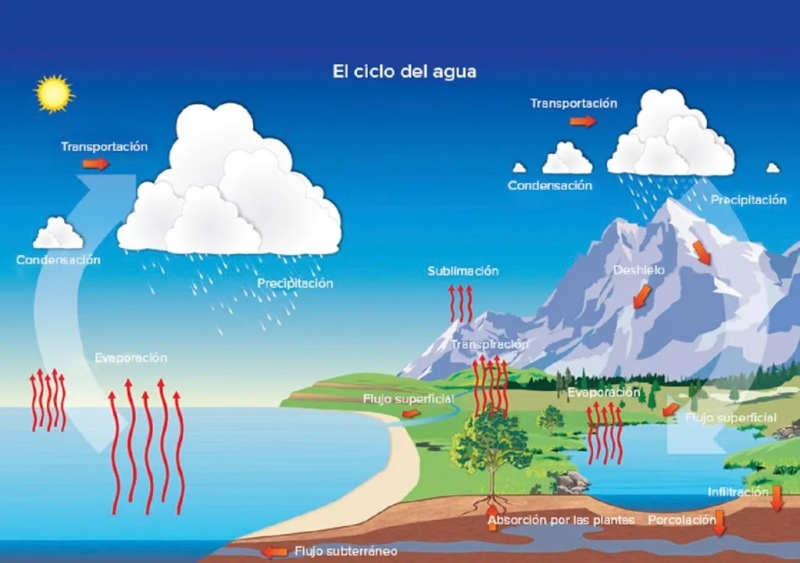
Lo principal del problema de la crisis del agua es comprender que el agua no se está acabando, la cantidad de agua que tenemos en la Tierra ha sido la misma siempre. Lo que ocurre es que la estamos contaminando, y en algunas partes ya no se encuentra a simple disposición. Esta es una de las consecuencias de la depredación de los ecosistemas (bosques y humedales, por ejemplo), que forman parte del ciclo del agua, filtran y también almacenan este recurso vital dejándolo limpio y en cantidades suficientes.
Por lo tanto, tenemos que frenar la contaminación del agua, debemos multiplicar la cantidad de vegetación y proteger los ecosistemas existentes.
Además, es muy necesario aprender sobre la administración y el uso consciente del agua. Según datos de la ONU, la industria textil es la responsable del 20% del agua contaminada del mundo; por ejemplo, para la fabricación de un pantalón de jean son necesarios entre 2 y 3 mil litros de agua, según un estudio realizado en la Universidad Politécnica de Madrid.
(Meteored)















